Kelompok Larutan Elektrolit Berupa Senyawa Ion, Kenali Sifat dan Contoh-Contohnya



PANGKALPINANG, Lintasbabel.iNews.id - Kelompok larutan elektrolit berupa senyawa ion, menjadi ulasan kita kali ini. Larutan elektrolit memiliki sifat yang bisa menghantarkan listrik. Larutan ini juga bisa berupa senyawa ion.
Larutan sendiri ada dua jenis yakni larutan elektrolit dan non-elektrolit. Larutan elektrolit adalah larutan yang zatnya dapat menghantarkan listrik saat dilarutkan ke dalam air, karena mengandung ion yang dapat bergerak bebas. Semakin banyak ion di dalam larutan, daya hantar listrik juga akan semakin kuat.
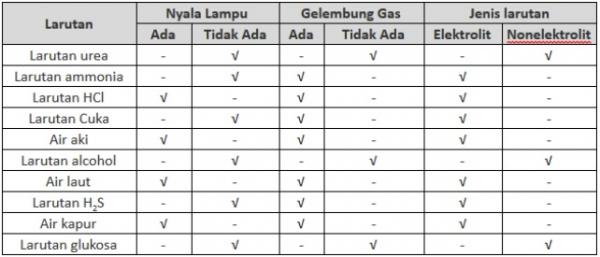
Sementara larutan non-elektorlit tidak dapat menghantarkan listrik, karena tidak ada ion-ion di dalamnya.
Larutan elektrolit disebut juga konduktor elektrik, yang terdiri atas 2 sifat, yakni larutan elektorlit kuat dan larutan elektrolit lemah.
Contoh larutan elektrolit kuat adalah:
Basa = KOH, NaOH, radium (Ra), dan basa dari golongan I A dan II A lainya (kecuali Be(OH)₂ dan Mg(OH)₂)
Asam = HCI, HBr, HI, HNO₃, HCIO₃, HCIO₄
Garam = NaCI, K₂SO₄, CaCI₂, AICI₃
Contoh larutan elektrolit lemah adalah:
Basa = Be(OH)₂, Mg(OH)₂, dan beberapa basa dari logam transisi.
Asam = HNO₂, H₃PO₃, H₃PO₄, H₂SO₃, HCN, H₂CO₃, HF
Senyawa ion sendiri dalah senyawa yang terdiri dari logam dan nonlogam yang memiliki ikatan ionik. Senyawa ini tidak dapat menghantarkan listrik jika kondisinya masih berbentuk padat. Namun, jika dilarutkan di dalam air maka akan mengalami ionisasi sempurna, sehingga dikategorikan sebagai elektrolit kuat, karena bisa menghantarkan listrik.
1. KOH (Kalium Hidroksida), potash kaustik
2. KCl (Kalium Klorida), garam kalium
3. K2SO4 (Kalium Sulfat), garaam abu sulfur
4. MgCl2 (Magnesium Klorida)
5. NaBr (Natrium Bromida)
6. NaCl (Natrium Klorida), garam

Itu tadi kelompok larutan elektrolit berupa senyawa ion, semoga bisa membantu kalian dalam memahami mata pelajaran Kimia di sekolah maupun di rumah. Selamat belajar!
Editor : Muri Setiawan