Sifat Koligatif Larutan: Pengertian, Manfaat dan Contoh Soal


PANGKALPINANG, Lintasbabel.iNews.id - Sifat Koligatif Larutan, pengertian, manfaat dan contoh soalnya bisa kamu temukan dalam artikel berikut ini. Koligatif Larutan merupakan salah satu materi dalam mata pelajaran Kimia tingkat SMA.
Dasar dari sifat koligatif terdapat dalam Hukum Roult, dimana koligatif berasal dari kata colligare yang berarti berkumpul bersama.
Dilansir dari buku Chemistry 10th Edition karya Raymond Chang, sifat koligatif larutan adalah sifat yang hanya bergantung pada jumlah partikel larutan dalam suatu larutan dan tidak bergantung pada sifat aalmi partikel terlarut.
Sifat koligatif larutan bergantung pada jumlah partikel terlarut saja, dalam bentuk atom, ion, maupun molekul. Jadi, semakin banyak zat terlarut, maka sifat koligatifnya juga akan semakin besar.
Sifat koligatif merupakan sifat yang hanya memandang jumlah atau kuantitas, bukan kualitas. Sifat larutan seperti rasa, warna, dan kekentalan (viskositas) merupakan sifat-sifat yang bergantung pada jenis zat terlarut.
Sifat-Sifat Koligatif Larutan
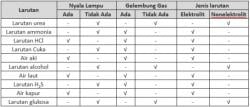
Terdapat dua jenis sifat koligatif larutan berdasarkan daya hantar listriknya, yakni sifat koligatif larutan elektrolit dan sifat koligatif larutan nonelektrolit.
Koligatif larutan elektrolit adalah larutan yang dapat menghantarkan arus listrik, contohnya NaCl (larutan garam). Sementara, koligatif larutan nonelektrolit tidak dapat menghantarkan arus listrik karena molekul-molekul terlarutnya tidak terionisasi di dalam larutannya, contohnya larutan gula seperti glukosa, sukrosa, larutan urea, dan lain sebagainya.
Rumus Sifat Koligatif Larutan Elektrolit
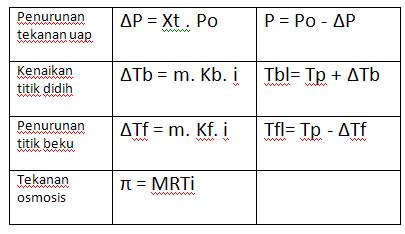
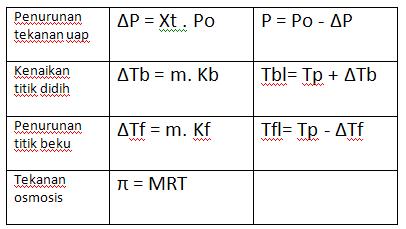
Keterangan:
Terdapat 4 macam sifat koligatif larutan, yaitu:
Beberapa manfaat sifat koligatif larutan adalah sebagai berikut:
1. Pembuatan Es Krim
Proses pembuatan es krim menerapkan prinsif sifat koligatif larutan yakni menggunakan garam untuk menurunkan suhu es. Hal ini agar es krim tidak mudah cair.
2. Cairan Infus
Prinsip sifat koligatif larutan pada cairan infus adalah tekanan osmotik larutan. Cairan infus dibuat dengan formulasi dan konsentrasi tertentu agar dapat masuk ke dalam tubuh menggantikan cairan yang hilang.
3. Mencairkan Salju
Penggunaan air garam dengan cara menaburkannya ke daerah bersalju, menerapkan prinsip sifat koligatif larutan. Larutan garam dapat menurunkan titik beku es, sehingga salju akan lebih cepat mencair
4. Membuat zat antibeku pada radiator mobil
Etilen glikol ditambahkan pada radiator mobil untuk menurunkan titik beku dan mencegah mesin mobil membeku lebih cepat. Hal ini hanya dilakukan di daerah atau negara dengan suhu dingin atau bersalju.
5. Antibeku dalam tubuh hewan
Zat antibeku dalam tubuh hewan di wilayah Kutub Utara dan Kutub Selatan bumi bermanfaat agar mereka bisa bertahan hidup di cuaca ekstrim.
1. Apa yang dimaksud dengan sifat koligatif larutan?
Jawaban:
Sifat larutan yang tidak bergantung pada jenis zat terlarut, tetapi bergantung pada jumlah partikel zat terlarut.
2. Larutan fruktosa dengan konsentrasi 1,476 M mempunyai massa jenis 1,2 g/ml. Berapa kemolala larutan adalah …. (Mr fruktosa = 180)
Jawaban:

3. Jika didalam suatu larutan yang dibuat dengan melarutkan 4,5 gram glukosa (C6H12O6) dalam 100 gram air, kemolalanya adalah …. (Ar C = 12, H =1, O = 16)
Jawaban:
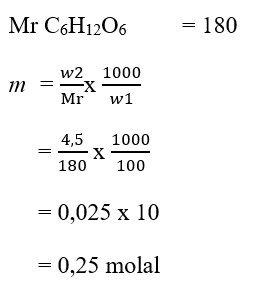
4. Jika suatu larutan mengandung 24 gram MgSO4 dilarutkan dalam 500 gram air.. molalitasnya adalah ….(Mr MgSO4 = 120)
Jawaban:

5. Di dalam suatu larutan yang telah dibuat dari 5 gram kristal NaOH yang dilarutkan ke dalam air hingga volumenya 500 mL, konsentrasinya adalah …. (Mr NaOH = 40)
Jawaban:

6. Jika di dalam suatu larutan yang dibuat dengan melarutkan 5,5 gram glukosa (C6H12O6) dalam 200 gram air,kemolalanya adalah …. (Ar C = 12, H =1, O = 16)
Jawaban:
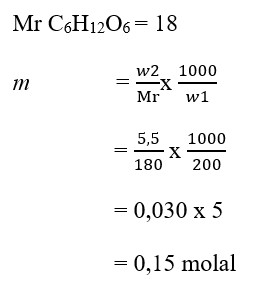
7. Sebanyak 11,7 gram NaCl (Mr = 58,5) dilarutkan dalam 500 gram air. Titik didih larutan adalah …. (Kb air = 0,52oC/m)
Jawaban:

8. Larutan elektrolit biner 5,85 gram dalam 500 gram membeku pada suhu -1,240C jika Kf air = 1,860C/m. Mr yang dibutuhkan adalah ….
Jawaban:

9. Larutan elektrolit biner 5,85 gram dalam 500 gram membeku pada suhu -1,240C jika Kf air = 1,860C/m. Mr yang dibutuhkan adalah ….
Jawaban:
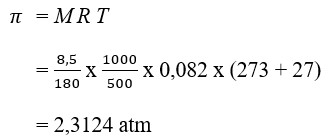
10. Dengan melarutkan 5 gram glukosa dalam 100 gram air, maka kemolalan larutan yang terbentuk (Ar C=12, H=1, O=16) adalah ….
Jawaban:
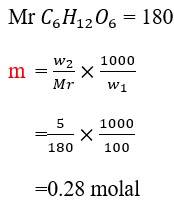
Demikianlah penjelasan tentang sifat koligatif larutan, pengertian, manfaat dan contoh soalnya. Semoga bermanfaat!
Editor : Muri Setiawan