Contoh Ikatan Ion


PANGKALPINANG, Lintasbabel.iNews.id - Contoh ikatan ion, wajib untuk diketahui oleh pelajar atau siswa SMA jurusan IPA. Ion sendiri dipelajari di mata pelajaran Kimia.
Untuk lebih jelasnya tentang ikatan ion, simak ulasan berikut ini sampai selesai, ya!
Pengertian Ikatan Ion
Ikatan ion adalah ikatan yang terjadi akibat adanya serah terima (tarik menarik) elektron, sehingga membentuk ion positif dan ion negatif yang konfigurasi elektronnya sama dengan gas mulia. Ikatan ini sisebut juga sebagai interaksi antara unsur yang mudah melepaskan elektron dan sulit melepaskan elektron melalui serah terima elektron.
Ion positif dan ion negatif diikat oleh suatu gaya yang dinamakan gaya elektrostatik. Nah, senyawa yang dihasilkan disebut dengan senyawa ion.
Penyebab terjadinya ikatan ion sendiri karena adanya perbedaan keelektronegatifan antara dua unsur, yakni unsur logam dan non logam. Unsur logam akan melepaskan elektron di kulit terluarnya, sehingga membentuk ion positif.
Elektron tersebut kemudian diterima oleh unsur nonlogam, hingga terbentuklah ion negatif.
Sementara, sifat dari senyawa ion adalah bersifat keras dan rapuh, titik didih dan titik lelehnya cukup tinggi, bisa larut di dalam air tetapi sulit untuk larut pada pelarut organik, serta bisa menghantarkan arus listrik pada fase cairnya.
Ciri-Ciri Ikatan Ion
Adapun ciri dari ikatan ion adalah sebagai berikut:
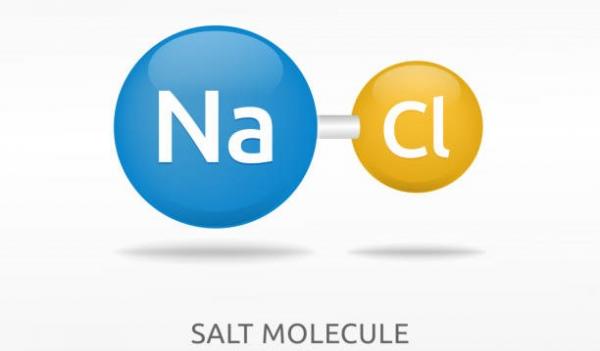
Contoh ikatan ion terdapat pada pasangan senyawa NaCl, KCl, dan Al2O3.
Ikatan ion pada NaCl terjadi antara unsur Na (golongan IA) dan unsur Cl (golongan VA). Adapun proses terbentuknya NaCl bisa kamu lihat pada konfigurasi berikut.
Reaksi pelepasan elektron: Na → Na+ + 1 e
Reaksi penangkapan elektron: Cl + e → Cl–
Berikut ini gambaran ikatannya:

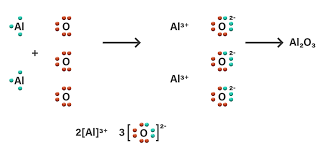
Ikatan ion pada Al2O3 terjadi antara unsur Al (golongan IIIA) dan unsur O (golongan VIA). Adapun proses terbentuknya Al2O3 bisa kamu lihat pada konfigurasi berikut.
Reaksi pelepasan elektron: Al → Al3+ + 3 e
Reaksi penangkapan elektron: O + 2e → O2-
Gambar ikatannya sebagai berikut:
Ikatan ion pada KCl terjadi antara unsur K (golongan IA) dan unsur Cl (golongan VA). Adapun proses terbentuknya KCl bisa kamu lihat pada konfigurasi berikut.
Reaksi pelepasan elektron: K → K+ + 1 e
Reaksi penangkapan elektron: Cl + e → Cl–
Perhatikan gambar berikut ini!
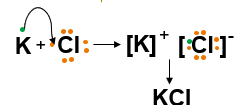
Demikian tadi ulasan tentang ikatan ion dan contohnya. Semoga bermanfaat!
Editor : Muri Setiawan